Hòa tan hết hỗn hợp A gồm 3,84 gam Mg và 2,16 gam Al vào dung dịch H2SO4 đặc, nóng, dư thu được 1,568 lít khí X (sản phẩm khử duy nhất) ở đktc. Gọi tên X.
Cho 9,2 gam hỗn hợp X gồm Mg và Fe vào dung dịch hỗn hợp AgNO3 và Cu(NO3)2, thu được chất rắn Y (gồm 3 kim loại) và dung dịch Z. Hòa tan hết Y bằng dung dịch H2SO4 (đặc, nóng, dư), thu được 6,384 lít khí SO2 (sản phẩm khử duy nhất của H2SO4, ở đktc). Cho dung dịch NaOH dư vào Z, thu được kết tủa T. Nung T trong không khí đến khối lượng không đổi, thu được 8,4 gam hỗn hợp rắn. Biết các phản ứng xảy ra hoàn toàn. Viết các phương trình phản ứng xảy ra và tính thành phần phần trăm khối lượng của các kim loại trong hỗn hợp ban đầu.
Hỗn hợp X gồm các kim loại Mg, Al, Zn. Lấy m gam hỗn hợp X tác dụng hết với dung dịch HCl dư thu được 6,72 lít khí (đktc). Cũng lấy m gam X tác dụng hết với dung dịch H 2 S O 4 đặc, nóng, dư thu được V lít khí S O 2 (sản phẩm khử duy nhất, ở đktc) và (m+a) gam muối. Giá trị của V và a lần lượt là
A. 3,36 và 28,8
B. 6,72 và 28,8
C. 6,72 và 57,6
D. 3,36 và 14,4
Hòa tan m gam hỗn hợp X gồm Fe2O3, CuO, MgO, FeO, Fe3O4 trong H2SO4 đặc nóng, dư, thu được 3,36 lít SO2 (đktc, sản phẩm khử duy nhất). Mặt khác, nung m gam X với khí CO dư, thu được chất rắn Y và hỗn hợp khí Z. Cho Z vào dung dịch Ca(OH)2 dư, sau khi phản ứng xảy ra hoàn toàn thu được 35 gam kết tủa. Hòa tan Y trong dung dịch HNO3 đặc nóng, due thu được V lít khí NO2 (sản phẩm khử duy nhất ở điều kiện tiêu chuẩn). Giá trị của V là:
A.33,6.
B. 11,2.
C. 44,8.
D. 22,4.
Hỗn hợp X gồm Mg, Zn, Cu và Al. Cho 14,7 gam X tác dụng với một lượng dư dung dịch HCl thu được 10,08 lít khí H2. Nếu hòa tan 14,7 gam X bằng một lượng dư dung dịch H2SO4 đặc, nóng thì thu được 10,64 lít khí SO2 (sản phẩm khử duy nhất ). Biết thể tích các khí đều đo ở đktc, các phản ứng xảy ra hoàn toàn. Tính phần trăm khối lượng của Cu có trong X .
Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\)
_ Khi tác dụng với HCl.
Ta có: \(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Theo ĐLBT mol e, có: 2a + 2b + 3d = 0,45.2 ⇒ 2a + 2b + 3d = 0,9 (1)
_ Khi tác dụng với H2SO4 đặc nóng.
Ta có: \(n_{SO_2}=\dfrac{10,64}{22,4}=0,475\left(mol\right)\)
Theo ĐLBT mol e, có: 2a + 2b + 2c + 3d = 0,475.2
⇒ 2a + 2b - 2c + 3d = 0,95 (2)
Trừ 2 vế của (1) và (2), có: c = 0,025 (mol)
\(\Rightarrow\%m_{Cu}=\dfrac{0,025.64}{14,7}.100\%\approx10,88\%\)
Bạn tham khảo nhé!
Đặt \(\left\{{}\begin{matrix}n_{Mg}=a\left(mol\right)\\n_{Zn}=b\left(mol\right)\\n_{Cu}=c\left(mol\right)\\n_{Al}=d\left(mol\right)\end{matrix}\right.\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\\n_{SO_2}=\dfrac{10,64}{22,4}=0,475\left(mol\right)\end{matrix}\right.\)
Bảo toàn electron: \(\left\{{}\begin{matrix}2a+2b+2c+3d=0,475\cdot2\\2a+2b+3d=0,45\cdot2\end{matrix}\right.\)
\(\Rightarrow2c=0,475\cdot2-0,45\cdot2=0,05\) \(\Rightarrow c=0,025\)
\(\Rightarrow\%m_{Cu}=\dfrac{0,025\cdot64}{14,7}\cdot100\%\approx10,88\%\)
Hòa tan hoàn toàn m gam hỗn hợp X gồm FeO, Fe(OH)2 và FeCO3 vào V lít dung dịch HNO3 1M, thu được dung dịch chỉ chứa một muối và 4,48 lít (đktc) hỗn hợp khí gồm CO2 và NO (sản phẩm khử duy nhất của N+5). Mặt khác, hòa tan hoàn toàn 0,15 mol X vào dung dịch H2SO4 (đặc, nóng, dư), thu được 2,8 lít (đktc) hỗn hợp khí gồm CO2 và SO2 (sản phẩm khử duy nhất của S+6. Giá trị của V là
A. 0,6.
B. 0,8.
C. 1,0.
D. 1,2.
Hòa tan hết 15,2 gam hỗn hợp hai kim loại Fe và Cu trong dung dịch H2SO4 đặc, nóng, dư, thu được 6,72 lít khí SO2 (sản phẩm khử duy nhất, ở đktc). Mặt khác cho 1,52 gam hỗn hợp vào dung dịch H2SO4 loãng dư thì thể tích khí thoát ra ở đktc là
A. 0,672 lít.
B. 2,24 lít.
C. 0,224 lít.
D. 0,448 lít.
Đáp án C
Trong 15,2 gam hỗn hợp kim loại
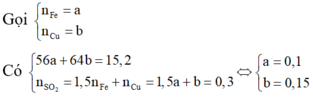
Do đó trong 1,52 gam hỗn hợp kim loại có 0,01 mol Fe.
Khi hòa tan 1,52 gam hỗn hợp kim loại vào dung dịch H2SO4 loãng dư thì nH = nF = 0,01
⇒ V H 2 = 0 , 224 ( lít )
Hỗn hợp rắn X gồm FeO và Fe3O4 có tỉ lệ mol 2:1. Dẫn khí CO đi qua m gam X nung nóng thu được 20 gam hỗn hợp rắn Y. Hòa tan hết Y vào dung dịch H2SO4 đặc nóng dư thu được 5,6 lít khí SO2 (đktc, sản phẩm khử duy nhất). Giá trị của m gần nhất với:
A. 22,5
B. 24,0
C. 20,5
D. 24,5
Đáp án A
Đặt nFeO = 2x mol; n F e 3 O 4 = x mol
→nFe = 2x+3x = 5x mol; nO = 2x+ 4x = 6x mol
20 gam hỗn hợp rắn Y có chứa Fe và O
→mO (trong Y) = mY - mFe = 20-5x.56 gam
→mO (đã phản ứng) = mO (X) - mO (Y) = 6x.16- (20-5x.56) = 376x-20 (gam)
→nO (đã phản ứng)= 376 x - 20 16 ( m o l ) = nCO pứ
CO+ m gam X→ 20 gam Y + H2SO4 đặc nóng dư→ Fe2(SO4)3+ SO2
Ta có: n S O 2 = 5,6/22,4 = 0,25 mol
- Quá trình cho e:
C+2 → C+4+ 2e
Fe→ Fe3++ 3e
5x → 15x mol
- Quá trình nhận e:
S+6+ 2e→ SO2
0,5← 0,25 mol
O + 2e →O-2
Bản chất phản ứng khử oxit sắt: CO + O(oxit) → CO2
Áp dụng định luật bảo toàn e: ne cho = ne nhận
→ 2 . 376 x - 20 16 +15x = 0,5+ 6x.2→ x = 0,06 mol
→m = 72.2x+ 232x = 22,56 gam
Hòa tan hoàn toàn 46,8 gam hỗn hợp chất X gồm R, RO, R3O4, R2O3 vào lượng dư dung dịch H2SO4 đặc nóng, thu được dung dịch Y và 8,96 lít khí SO2 (là sản phẩm khử duy nhất của S+6, ở đktc). Cô đặc dung dịch Y, rồi làm lạnh, thu được 225,54 gam muối Z kết tinh với hiệu suất đạt 90%. Xác định R và công thức của muối Z, biết hằm lượng oxi có trong X là 22,222%.
Quy đổi X thành hai nguyên tố R (x mol) và O (y mol).
nSO2 = 8,96/22,4 = 0,4 (mol)
Quá trình khử:
S+6 + 2e ---> S+4
0,8 <-- 0,4
O0 + 2e ----> O-2
y -> 2y
Quá trình oxi hóa:
R0 ----> R+3 + 3e
x --------------> 3x
Áp dụng định luật bảo toàn e:
0,8 + 2y = 3x (1)
Ta lại có:
mO2/mhh . 100% = 22,222%
<=> mO2/46,8 = 0,22222
=> mO2 \(\approx\) 10,4 (g)
=> y = nO2 = 10,4/16 = 0,65 (mol)
Thế y vào (1) ta được x = 0,7 (mol)
mR = 46,8 - 10,4 = 36,4 (g)
=> MR = 36,4/0,7 = 52 (g/mol)
=> R là Cr.
Hỗn hợp X gồm Mg và Al. Cho 0,75 gam X phản ứng với HNO3 đặc, nóng, dư, thu được 1,568 lít NO2 (sản phẩm khử duy nhất ở đktc), tiếp tục cho thêm dung dịch NaOH dư vào, sau khi các phản ứng hoàn toàn thu được m gam kết tủa. Giá trị của m là
A. 0,78 gam
B. 1,16 gam
C. 1,49 gam
D. 1,94 gam